Korrosion
Ordet korrosion kommer av det latinska verbet corrodere som
betyder sönderfräta. Stål/järn vill övergå till sitt normala tillstånd som
är rost eller malm och korrosionshastigheten påverkas av försurningen från
svaveldioxid (gas från oljeförbränning) och klorider (salter) från t.ex.
havsvatten. Om saltet från "västkustregn" ej avtvättas så ökas korrosionen.
Järn och stål rostar, koppar ärgar, zink får vitblemma och aluminium får
vita korrosionsprodukter!
Ej vetenskaplig test av korrosion!
Galvanisk spänningsserie, redovisad som
Elektrodpotential
es, volt för metaller i
seawater/havsvatten vid
+20 grader Celsius.
A. Galvanisk korrosion är ett elektrokemiskt fenomen. Om två olika metaller kommer i kontakt med
varandra och det finns fukt och syre mellan dem så startar en strömkälla.
Strömvandringen sker om skillnaden i elektropotential är minst 0,05 Volt. Ju högre potentialskillnaden
är mellan materialen ju fortare börjar den oädlaste
metallen "rosta", flytta över till den ädlare metallen. Anod går till Katod!
Rost. För att skydda stålet mot rost som fås när järnet kommer i kontakt med vatten innehållande syre, belägges plåten med ett
fukt & vattentätt zinkskikt på mellan 20-25 my. Det räcker dock inte bara med
ett skyddande zinkskikt mot korrosion, utan plåten måste också kontinuerligt
målas, då zink också korroderar med ca 0,5 - 10
my/år. Täckfärg för plåtslageriändamål
är också fuktgenomsläpplig varför man först måste måla plåten med en
fuktupptagande färg. Färgen kan också bli vattengenomsläpplig om skador skett
på ytskiktet.
Ett sätt att hindra rost skulle vara att tillsätta C-vitamin i
vattnet, som tar bort syret, vilket då skulle innebära att rost ej kan
uppträda. Dock finns vissa praktiska och ekonomiska problem med den
lösningen. Eller så skulle man se till att den Relativa Fuktigheten inte
överstiger 50%, för då rostar inte metaller järn och stål.
Kromatering
Förzinkade plåtytor har dåligt korrosionsskydd och korroderar lätt i
fuktig miljö och bildar vitrost eller vitblemma. t.ex. vid transporter och
lagring. Förr anoljades plåten, från 1960 till 2000-talet doppades plåten i en
blandning som innehåller krom Cr6 och sedan 2006 i Cr3+. Lösningen reagerar
med zinken och låter lite zink och bildar ett tunt skyddsskikt kallad
kromatering.
Ett kromateringsskikt förbättrar glansen, ger vitrostskydd och skyddar mot
rödrost som framträder när svavelhaltig luft påverkar zinkskiktet.
När plåten fått en sträv yta av att zinken exponeras i luften och bildat
zinkkarbonat, kan plåten målas.
OBS. Sedan 2006 med krom Cr3+ tar det längre tid, 2-10 år innan
kromskiktet är borta, om det överhuvudtaget försvinner!
Testa om det finns krom kvar på plåt!
Stålindustrin arbetar med
att ersätta kromateringen med harmlösare skydd mot vitrost.
Regnskugga, är ett korrosionsfenomen som kan inträffa
på undersidan av plåt, t.ex. på plåt som är monterad i undertaket på en genomgång till
gården eller på undersidan av ett skärmtak, och där man har mycket fukt beroende på "ett ständigt regnande" som på västkusten!
Åtgärdas med ökad ventilation eller utbyte av material till exempelvis
puts!
B. Spaltkorrosion, är ett fenomen som
kan uppträda t.ex. i falser om fals ständigt står under vatten eller är utsatt
för långvarig kondens! Detta kan också gälla när två plåtar ligger nära varandra
eller att plåt är knäckt, veckad eller liknande - om den står under vatten eller
är utsatt för ständig kondens!
Korrosion på färgbelagd förzinkad plåt
Förzinkad plåt är självläkande och normalt bildas en galvanisk cell runt
en skada på zinkskiktet och "lagar" sig själv. Zinken blir en
offeranod "offrar sig" och skyddar stålet mot korrosion. Korrosionen
är högre
på en horisontell yta än på en vertikal yta.
Men detta gäller inte när plåten är belagd med färg,
antingen platsmålad eller fabrikslackerad. Då sker följande vid en skada
på zinkskiktet: stålet rostar och rosten kryper in under omgivande
färgskikt och lyfter bort färgen. Korrosionen fortsätter tills plåten rostat
sönder.
C.
Zinkavfrätning/ atmosfärisk korrosion
Zink isolerar stålytan, dock
är
zinken oädlare och korroderar långsammare än stål. Det är orsaken till att zink användes till att förlänga livslängden på järn och stål, med minst 5 gånger!
Zinken offrar sig och
fördröjer därmed korrosion i stålytan
Nedanstående tabell och diagram visar avfrätning per
år och hur lång livslängden beräknas vara, i olika miljöer. Grönt område gäller för plåt till byggnadsplåtslageri. Lantbruk med djur och gödselhantering
innehållande ammoniak skall jämföras med Industrimiljö.
Zinkavfrätning:
| Område |
my/år |
| Inomhus |
<0,5 |
| Fjäll |
<1,0 |
| Landet |
1,0 |
| Byar |
1,5 |
| Städer |
2,0 |
| Kuster |
3,0 |
| Storstad |
5,0 |
| Industrimiljö
| 10,0 |
| Sötvatten |
20,0 |
| Saltvatten |
50,0 |
|
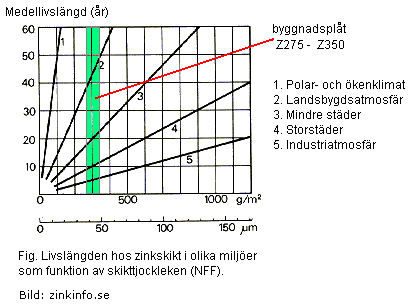 |
Notera att diagrammet visar att skikttjockleken i området 275-350 g/m2
skall vara mellan 35 och 50 my.
Luftens halt av svaveldioxid har dock minskat kraftigt sedan 2000-talet
och då också zinkens korrosion, så värdena ovan är lite höga!
Uppgifterna kommer från Nordisk Förzinkningsförening (NFF) och Hus-AMA
Korrosivitetsklasser:
| Korrosivitets-/Miljöklasser |
Krav på beläggning av
stålplåt |
eller annat material |
| C5 / M4 - tuff industrimiljö
| Z275 + 300
my platsmålning |
Rostfritt |
| C4 / M3 - större städer, kuster |
Z275 + 25
my plastbeläggning
alt. + 160 my platsmålning
|
Rostfritt*
Aluminium
Aluzink |
| C3 / M2 - inlandet |
Z275 (275g/kvm zink) |
Rostfritt
Aluminium
Aluzink |
* Vid en incidens i en simhall i Örebro omkring 1990,
ramlade
ventilationskanalerna ned!
De var upphängda med rostfria plåtband.
Idag är de utbytta mot förzinkade plåtband.
En ny incidens inträffade i samma simhall år 2007, då blomlådor
upphängda i rostfria ringar, ramlade ned!
Dagens moderna upplevelsesimhallar med hög badvattentemperatur,
hög relativ fuktighet, desinfektionskemikalier och hög koncentrationen av
klor ställer höga krav på det rostfria materialet. Rening med Ozon har inte samma påverkan som Klor!